
Interpretación del Antibiograma Sugerido para Staphylococcus Gram Positivo
Una guía detallada para entender la sensibilidad antibiótica de Staphylococcus
Como AI asistente, Ithy se basa en la agregación de información de múltiples modelos de lenguaje y fuentes para ofrecer respuestas completas y estructuradas. En este caso, proporcionaremos una descripción detallada del antibiograma sugerido para Staphylococcus, un coco Gram positivo de gran relevancia clínica, integrando conocimientos sobre su identificación, mecanismos de resistencia y opciones de tratamiento.
Aspectos Clave del Antibiograma para Staphylococcus
- Identificación: La confirmación de Staphylococcus se realiza mediante pruebas como la tinción de Gram (cocos Gram positivos en racimos) y pruebas bioquímicas (catalasa y coagulasa).
- Resistencia a Meticilina: La detección de la resistencia a meticilina (SARM) es fundamental para la elección del tratamiento, ya que implica resistencia a todos los betalactámicos, excepto ceftobiprol y ceftarolina.
- Opciones de Tratamiento: La vancomicina, daptomicina y linezolid son antibióticos clave para el tratamiento de infecciones por SARM, aunque la elección específica dependerá de la gravedad y el tipo de infección.
Identificación de Staphylococcus
El género Staphylococcus agrupa bacterias cocáceas Gram positivas que tienden a agruparse en racimos, lo que las diferencia de otros cocos Gram positivos como Streptococcus, que se presentan en cadenas. La identificación inicial en el laboratorio implica:
Tinción de Gram
La observación microscópica de una muestra teñida con Gram revelará la morfología característica de cocos violetas (Gram positivos) agrupados. Este es el primer paso para sospechar una infección por Staphylococcus.
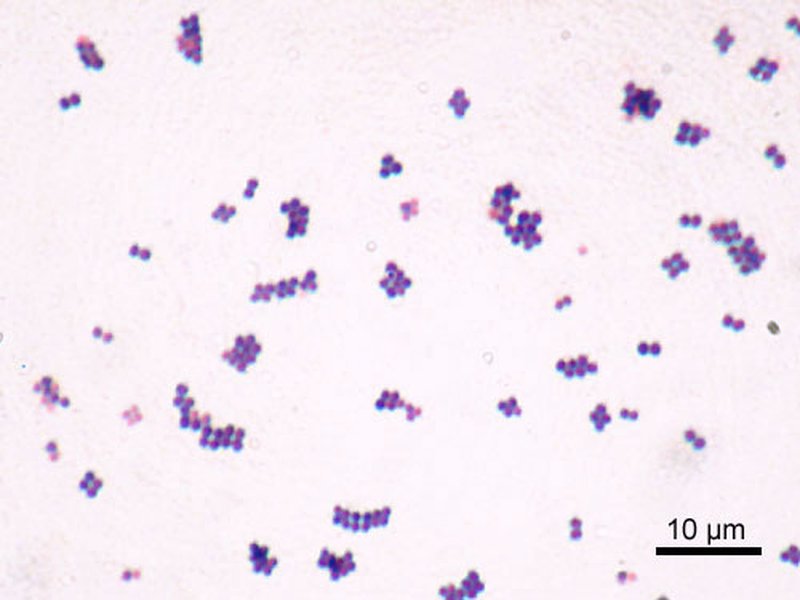
Micrografía de Staphylococcus aureus teñido con Gram
Pruebas Bioquímicas
Para diferenciar las especies de Staphylococcus, se realizan pruebas bioquímicas. La prueba de la catalasa es positiva para Staphylococcus (diferenciándolo de Streptococcus). La prueba de la coagulasa es crucial para distinguir entre Staphylococcus aureus (coagulasa positivo) y los estafilococos coagulasa negativos (ECN), como Staphylococcus epidermidis y Staphylococcus saprophyticus, que tienen diferente relevancia clínica y patrones de sensibilidad.

Identificación de Staphylococcus mediante cultivo y prueba de coagulasa
La Importancia del Antibiograma en Staphylococcus
Las infecciones por Staphylococcus aureus son frecuentes y pueden variar en gravedad, desde infecciones cutáneas leves hasta bacteriemias y neumonías que ponen en riesgo la vida. La emergencia de cepas resistentes a los antibióticos, particularmente el Staphylococcus aureus resistente a meticilina (SARM), hace que el antibiograma sea una herramienta indispensable para guiar el tratamiento adecuado.
Principales Mecanismos de Resistencia en Staphylococcus
Resistencia a Betalactámicos (Resistencia a Meticilina - SARM)
El mecanismo de resistencia a betalactámicos más relevante en Staphylococcus es la adquisición del gen mecA, que codifica una proteína de unión a penicilina alterada (PBP2a) con baja afinidad por los antibióticos betalactámicos. Esta resistencia confiere resistencia a la meticilina, oxacilina, nafcilina y a la mayoría de las cefalosporinas, con la excepción de las nuevas cefalosporinas ceftobiprol y ceftarolina. La detección de SARM es crucial y se realiza mediante pruebas fenotípicas (sensibilidad a oxacilina o cefoxitina) o genotípicas (detección del gen mecA).
\[ \text{Gen } mecA \rightarrow \text{PBP2a alterada} \rightarrow \text{Resistencia a la mayoría de los Betalactámicos} \]
Resistencia a Glicopéptidos (Vancomicina)
Aunque la vancomicina es un pilar en el tratamiento de SARM, han surgido cepas con sensibilidad disminuida (VISA - Vancomycin-Intermediate Staphylococcus aureus) y, raramente, cepas resistentes (VRSA - Vancomycin-Resistant Staphylococcus aureus). La resistencia a vancomicina puede ser homogénea (CMI elevadas) o heterogénea (hVISA - heterogeneous Vancomycin-Intermediate Staphylococcus aureus, con subpoblaciones resistentes no detectadas por los métodos estándar de difusión).
Resistencia a Macrólidos y Lincosamidas (MLSB)
La resistencia a macrólidos, lincosamidas y estreptograminas B (MLSB) es común en Staphylococcus y puede ser constitutiva o inducible. La resistencia inducible a clindamicina en cepas resistentes a eritromicina es importante, ya que la clindamicina puede parecer sensible in vitro pero fracasar terapéuticamente in vivo. El D-test es una prueba fenotípica para detectar la resistencia inducible a clindamicina.
Antibiograma Sugerido para Staphylococcus
Un antibiograma para Staphylococcus debe incluir un panel de antibióticos que permita identificar los mecanismos de resistencia más relevantes y guiar la selección terapéutica. La interpretación de los resultados debe considerar si la cepa es sensible o resistente a meticilina (SARM o SASM - Staphylococcus aureus sensible a meticilina).
Panel de Antibióticos Sugerido
| Clase de Antibiótico | Antibióticos Representativos | Relevancia en el Antibiograma |
|---|---|---|
| Betalactámicos | Oxacilina o Cefoxitina, Penicilina, Cefazolina, Amoxicilina-Clavulánico | Detección de resistencia a meticilina (gen mecA), sensibilidad a penicilina (producción de penicilinasa). |
| Glicopéptidos | Vancomicina, Teicoplanina | Tratamiento de elección para SARM. Monitoreo de CMI para detectar sensibilidad disminuida (VISA, hVISA). |
| Lincosamidas | Clindamicina | Evaluación de resistencia (MLSB). Importante realizar D-test si hay resistencia a macrólidos. |
| Macrólidos | Eritromicina | Detección de resistencia a macrólidos, lo que puede indicar resistencia inducible a clindamicina. |
| Aminoglucósidos | Gentamicina, Tobramicina | Puede ser útil en terapia combinada para infecciones graves. La resistencia a tobramicina puede ser un marcador de resistencia a otros betalactámicos. |
| Quinolonas | Ciprofloxacino, Levofloxacino | La resistencia es común, especialmente en SARM. |
| Sulfonamidas | Trimetoprima/Sulfametoxazol (TMP/SMX) | Buena actividad contra muchos SARM de adquisición comunitaria. |
| Tetraciclinas | Tetraciclina, Doxiciclina, Minociclina | Actividad contra muchas cepas de SARM. |
| Oxazolidinonas | Linezolid | Alternativa a vancomicina para SARM, especialmente en neumonía. Monitoreo de resistencia emergente. |
| Lipopéptidos | Daptomicina | Alternativa a vancomicina para SARM, especialmente en bacteriemia. No usar para neumonía. |
| Glicilciclinas | Tigeciclina | Actividad contra SARM, pero con limitaciones en ciertas infecciones. |
| Nuevas Cefalosporinas | Ceftarolina, Ceftobiprol | Activas contra SARM. |
Interpretación del Antibiograma
Staphylococcus sensible a Meticilina (SASM)
Las cepas SASM suelen ser sensibles a la mayoría de los antibióticos betalactámicos, como oxacilina, nafcilina, cefazolina, amoxicilina-clavulánico y piperacilina-tazobactam. El tratamiento de elección para infecciones graves por SASM es un betalactámico antiestafilocócico intravenoso (por ejemplo, nafcilina o cefazolina).
Staphylococcus aureus resistente a Meticilina (SARM)
Las cepas de SARM son resistentes a los betalactámicos. El tratamiento debe basarse en antibióticos activos contra SARM. Las opciones principales incluyen vancomicina, daptomicina, linezolid, tigeciclina, trimetoprima/sulfametoxazol, clindamicina (si D-test negativo) y las nuevas cefalosporinas activas contra SARM.
La elección del antibiótico para SARM depende de varios factores, incluyendo la gravedad y localización de la infección, la sensibilidad demostrada en el antibiograma, la farmacocinética/farmacodinámica del fármaco en el sitio de la infección y las condiciones del paciente (función renal, interacciones medicamentosas).
Por ejemplo:
-
Para infecciones cutáneas no complicadas por SARM adquirido en la comunidad, trimetoprima/sulfametoxazol o clindamicina (si sensible) pueden ser opciones orales.
-
Para infecciones graves por SARM, como bacteriemia o neumonía, vancomicina, daptomicina o linezolid son los tratamientos de elección por vía intravenosa.
Consideraciones Adicionales en la Interpretación del Antibiograma
Lectura Interpretada
La lectura interpretada del antibiograma va más allá de simplemente informar si un microorganismo es sensible, intermedio o resistente a un antibiótico. Implica analizar los patrones de resistencia para inferir posibles mecanismos de resistencia y predecir la respuesta terapéutica. Por ejemplo, una cepa de Staphylococcus resistente a eritromicina pero sensible a clindamicina requiere un D-test para descartar resistencia inducible a clindamicina.
Variabilidad Geográfica y Temporal
La prevalencia de los mecanismos de resistencia puede variar geográficamente y cambiar con el tiempo. Es importante que los laboratorios de microbiología realicen vigilancia local de la resistencia y que los clínicos estén al tanto de los patrones de resistencia en su área.
Correlación Clínico-Microbiológica
La interpretación del antibiograma debe hacerse siempre en el contexto clínico del paciente. La sensibilidad in vitro no siempre garantiza el éxito terapéutico in vivo, y factores como la concentración del antibiótico en el sitio de la infección, el estado inmunológico del paciente y la presencia de cuerpos extraños pueden influir en el resultado.
Video Relacionado
El siguiente video ofrece una explicación detallada sobre la lectura interpretada del antibiograma en cocos Gram positivos, lo cual es fundamental para comprender el significado de los resultados obtenidos para Staphylococcus.
Lectura interpretada del antibiograma en Gram positivos
Preguntas Frecuentes
¿Qué significa SARM?
SARM significa Staphylococcus aureus resistente a meticilina. Son cepas de Staphylococcus aureus que han desarrollado resistencia a los antibióticos betalactámicos, incluyendo la meticilina, oxacilina y la mayoría de las cefalosporinas, debido a la presencia del gen mecA.
¿Por qué es importante realizar un antibiograma para una infección por Staphylococcus?
Es crucial realizar un antibiograma para determinar la sensibilidad de la cepa de Staphylococcus a diferentes antibióticos. Esto permite seleccionar el tratamiento más efectivo y evitar el uso de antibióticos a los que la bacteria es resistente, lo que podría llevar al fracaso terapéutico y al desarrollo de más resistencia.
¿Cuáles son los principales antibióticos utilizados para tratar infecciones por SARM?
Los principales antibióticos utilizados para tratar infecciones graves por SARM incluyen vancomicina, daptomicina y linezolid. Otras opciones pueden ser tigeciclina, trimetoprima/sulfametoxazol y clindamicina (si la cepa es sensible).
¿Qué es el D-test?
El D-test es una prueba de laboratorio que se realiza en cepas de Staphylococcus resistentes a eritromicina pero sensibles a clindamicina. Detecta la resistencia inducible a clindamicina, que si no se identifica, puede llevar al fracaso del tratamiento con clindamicina.
¿Puede una infección por Staphylococcus tratarse sin antibióticos?
En algunos casos de infecciones cutáneas leves por Staphylococcus, como forúnculos pequeños, el drenaje del absceso puede ser suficiente. Sin embargo, la mayoría de las infecciones por Staphylococcus requieren tratamiento antibiótico para su resolución, especialmente si son más graves o invasivas.
Referencias
Last updated May 16, 2025