
Cre-lox 重組系統的精妙:Brainbow、DIO 和 DO 的運作機制
探索基因表達的精確控制與神經元多彩成像的科學奧秘
Cre-lox 重組系統是基因工程領域中一個極為強大且靈活的工具,它允許科學家對基因表達進行精確的時空控制。這個系統的核心是兩種成分:來自 P1 噬菌體的 Cre 重組酶(Cre recombinase)和其特定的識別位點 loxP。藉由巧妙設計 loxP 位點的排列和方向,Cre 酶能夠在 DNA 上執行多種操作,包括刪除(deletion)、插入(insertion)、轉位(translocation)和反轉(inversion)。這些操作為研究基因功能、疾病模型建立以及細胞追蹤提供了前所未有的可能性,尤其在神經科學領域,它催生了如 Brainbow 這樣能夠以多種顏色標記細胞的創新技術。
關鍵亮點:Cre-lox 系統與其多樣化應用
- Cre-lox 基礎: 該系統由 Cre 重組酶和 loxP 位點組成,能夠在 DNA 上執行刪除、反轉、插入和轉位等操作,實現對基因表達的精確控制。
- Brainbow 系列技術: Brainbow 1.0、2.0 和 3.0 利用 Cre-lox 系統的隨機重組特性,在單一細胞中表達不同比例的螢光蛋白,從而為個別神經元賦予獨特的顏色,極大地促進了神經迴路的可視化研究。
- DIO 與 DO 開關: DIO (Double-floxed Inverted Orientation) 和 DO (Double-floxed Orientation) 向量是 Cre-lox 系統中用於控制基因「開啟」或「關閉」的關鍵機制。DIO 向量在 Cre 存在時反轉基因方向使其表達(Cre-On),而 DO 向量則在 Cre 存在時反轉基因方向使其停止表達(Cre-Off)。
Cre-lox 重組系統的基礎原理
Cre-lox 系統的核心是 Cre 重組酶和 loxP 位點。Cre 重組酶是一種來自 P1 噬菌體的 38 kDa 蛋白質,它能夠識別並結合到 loxP 位點上。loxP 位點是一個 34 個鹼基對(bp)的 DNA 序列,由兩個 13 bp 的反向重複序列和一個 8 bp 的非對稱間隔區組成。這個 8 bp 的間隔區賦予了 loxP 位點方向性,這對於決定 Cre 介導的重組結果至關重要。
當 Cre 酶識別並結合到兩個 loxP 位點時,它會形成一個四聚體複合物,並催化這兩個位點之間的 DNA 重組。重組的結果取決於 loxP 位點在 DNA 上的相對方向:
- 同向排列(Directly Oriented): 如果兩個 loxP 位點以相同方向排列,Cre 酶會切除這兩個位點之間的 DNA 片段,導致 DNA 缺失。
- 反向排列(Oppositely Oriented): 如果兩個 loxP 位點以相反方向排列,Cre 酶會反轉這兩個位點之間的 DNA 片段。
這種機制不需要額外的輔助蛋白或能量因子,並且在多種生物體中都有效,包括細菌、酵母、植物和哺乳動物細胞,尤其在基因工程小鼠模型中應用廣泛。
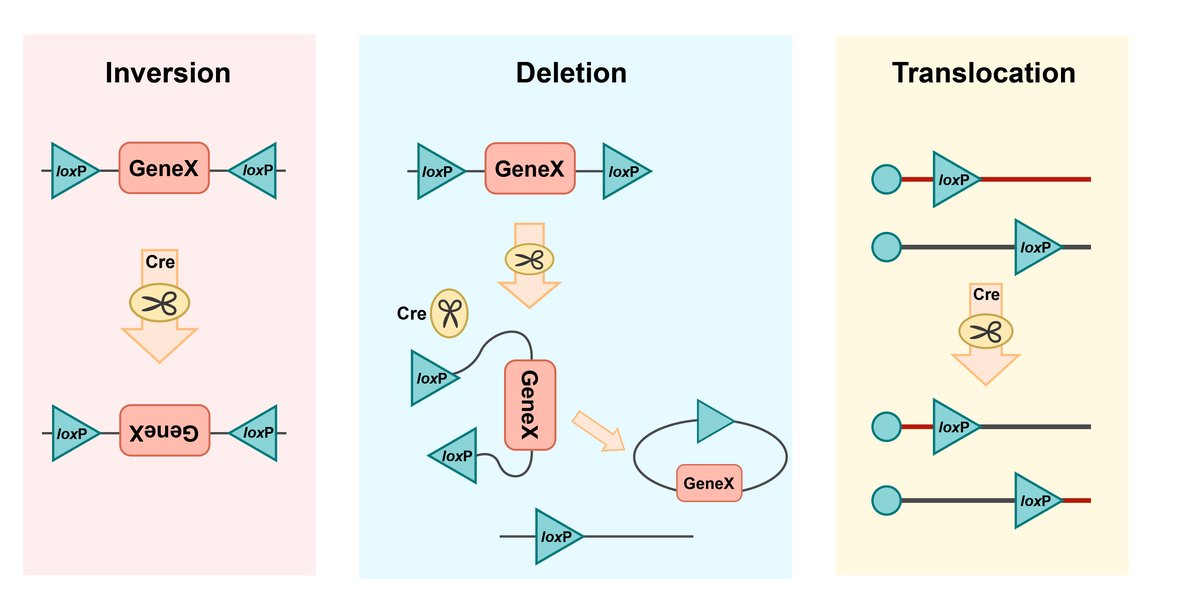
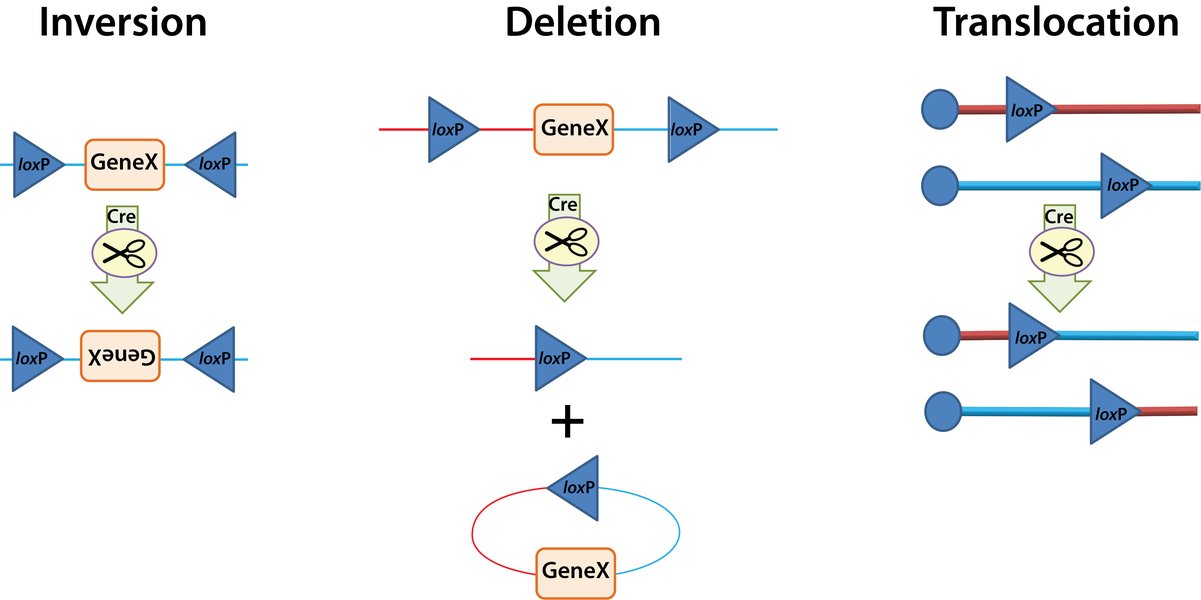
Cre-lox 重組系統的基本機制。圖片展示了 Cre 重組酶如何作用於 loxP 位點,導致 DNA 的切除或反轉。
Brainbow 技術:神經元的多彩成像
Brainbow 是一種革命性的技術,它利用 Cre-lox 重組系統來隨機且獨特地標記個別細胞,尤其是神經元,使其呈現出多種螢光顏色。這使得研究人員能夠在複雜的神經網路中區分和追蹤單個細胞及其錯綜複雜的連接。Brainbow 技術的發展是對傳統單一螢光標記技術的重大改進,它為神經迴路的可視化提供了前所未有的細節。
Brainbow 1.0:基於互斥性切除的顏色隨機組合
Brainbow 1.0 的設計策略是利用不同突變型 loxP 位點之間的互斥性重組。它包含多個螢光蛋白基因(例如 RFP, YFP, M-CFP),這些基因由不同類型的 loxP 位點(如 loxP, lox2272, loxN)分隔開來。這些 loxP 位點被巧妙地交錯排列,使得 Cre 酶只能在相同類型的 loxP 位點之間進行重組。當 Cre 酶存在時,會發生隨機的 DNA 切除事件。由於這些切除是互斥的,每個細胞最終只會表達一個特定的螢光蛋白,或是不同螢光蛋白的組合,從而產生多種獨特的顏色。
在 Brainbow 1.0 的構建中,通常有三個或四個螢光蛋白(XFPs)被整合到一個轉基因中。例如,Brainbow-1.0 包含 RFP(紅色)、YFP(黃色)和 M-CFP(膜結合青色螢光蛋白)。在沒有 Cre 重組酶的情況下,通常會表達最前端的螢光蛋白(例如 RFP)。當 Cre 存在時,它會介導兩種可能的刪除事件,從而導致 YFP 或 M-CFP 的表達。這些刪除事件是由兩種不同的 loxP 變體所定義,只有相同的 loxP 位點之間才能發生重組。這創造了一個隨機選擇表達特定螢光蛋白的機會,因為每個細胞中的 Cre 重組事件是隨機發生的。
這種隨機性使得鄰近的細胞可以表達不同的螢光蛋白組合,從而在顯微鏡下呈現出獨特的顏色。雖然 Brainbow 1.0 提供了一定程度的顏色多樣性,但其主要限制在於可生成的顏色數量相對有限,因為它依賴於單一的隨機切除事件。
Brainbow 2.0:利用反轉和切除事件增加顏色複雜度
Brainbow 2.0 的設計則引入了基因片段的反轉(inversion)機制,以進一步增加顏色組合的複雜性。與 Brainbow 1.0 的單一切除策略不同,Brainbow 2.0 利用反向排列的 loxP 位點來介導 DNA 片段的反轉。它通常包含兩個螢光蛋白的編碼序列,這些序列以相反方向排列在一個由內向的 loxP 位點側翼的可反轉盒中。當 Cre 酶存在時,這個盒狀結構可以不斷地反轉,直到 Cre 酶活性停止,然後它會隨機穩定在某個方向上,從而決定哪個螢光蛋白會被表達。
以 Brainbow-2.0 為例,它包含一個可反轉的盒狀結構,其中兩個 XFP 基因以頭對頭的方式排列。只要 Cre 酶持續活躍,這個結構就可以持續反轉。當 Cre 酶活性終止時,它會隨機穩定在一個方向上,導致其中一個 XFP 基因被表達。Brainbow-2.1 則包含兩個相鄰的此類盒狀結構,進一步增加了可能的反轉和切除事件,從而產生更多的顏色變體。
透過結合反轉和切除事件,Brainbow 2.0 能夠在給定的構建中實現多種表達可能性。這種方法使得細胞能夠表達多達四種不同的螢光蛋白之一,具體取決於 Cre 介導的切除和反轉組合。這種策略提高了可識別細胞的顏色多樣性,為神經元的可視化提供了更豐富的細節。
Brainbow 3.0:改進的螢光蛋白與 Brainbow 1.0 格式的結合
Brainbow 3.0 延續了 Brainbow 1.0 的 loxP 位點排列格式,但其關鍵改進在於替換了原有的螢光蛋白,使用了毒性更低、亮度更高、光穩定性更好的新一代螢光蛋白,例如 mOrange2、EGFP 和 mKate2。這種改進旨在提高成像質量,同時降低螢光蛋白對細胞生理功能的潛在影響。Brainbow 3.0 仍然依賴於不相容的 loxP 突變體之間的隨機重組和切除,以實現多色標記。儘管基礎的重組機制與 Brainbow 1.0 類似,但更優異的螢光蛋白使得細胞標記更加清晰和穩定。
Brainbow-3.0 轉基因品系整合了 mOrange2、EGFP 和 mKate2 的法尼基化衍生物。它保留了 Brainbow 1 的格式,其中不相容的野生型和突變型 lox 位點被連接起來,這樣 Cre 重組酶就可以在 XFPs 之間進行隨機選擇。這種對螢光蛋白的優化,使得 Brainbow 3.0 在實際應用中具有更好的性能,為神經元的精細結構和連接提供更清晰的圖像。
此影片深入淺出地解釋了 Cre/Lox 系統的工作原理及其在 Brainbow 技術中的應用。
Cre-lox 系統在基因表達控制中的應用:DIO 與 DO 開關
除了多色成像,Cre-lox 系統在精確控制特定細胞或組織中的基因表達方面也發揮著關鍵作用。DIO (Double-floxed Inverted Orientation) 和 DO (Double-floxed Orientation) 向量是實現這種控制的兩種主要策略,它們允許研究人員根據 Cre 重組酶的存在與否來「開啟」或「關閉」特定基因的表達。
DIO (Double-floxed Inverted Orientation) 向量:Cre-On 開關
DIO 向量,又稱為「雙側翼反向開放閱讀框(Double-floxed Inverted Open Reading Frame, FLEx)」向量,是一種「Cre-On」系統。在這種設計中,目標基因(Gene of Interest, GOI)被反向(3'->5')克隆,並由兩對不同類型的 loxP 位點側翼,例如 loxP 和 lox2272。重要的是,這兩對 loxP 位點是相互不相容的,即 loxP 只能與 loxP 重組,lox2272 只能與 lox2272 重組。
在 Cre 存在時:
當細胞中表達 Cre 重組酶時,Cre 會識別並結合其中一對 loxP 位點(例如 loxP 對),並介導其間 DNA 片段的反轉。一旦發生第一次反轉,目標基因就會從反向(不表達)變為正向(5'->3'),從而可以被轉錄和翻譯。在第一次反轉後,第二對 loxP 位點(例如 lox2272)現在會位於兩個 loxP 位點之間,導致其被 Cre 酶切除。這種機制確保了目標基因一旦被「開啟」,就無法再反轉回非表達狀態。因此,DIO 向量只有在 Cre 酶存在時才允許基因表達,實現了高度特異性的「Cre-On」功能。
在 Cre 不存在時:
如果細胞中沒有 Cre 重組酶,或者 Cre 活性不足,那麼目標基因將保持其反向排列。由於基因的反向排列,它無法被正確地轉錄和翻譯,因此基因表達會被抑制。這使得 DIO 向量成為在特定細胞類型或特定時間點精確激活基因表達的理想工具。
DIO 向量(Cre-On)的運作原理。在 Cre 存在時,反向的基因序列會被反轉為正向,從而開啟基因表達。
DO (Double-floxed Orientation) 向量:Cre-Off 開關
與 DIO 向量相反,DO 向量是一種「Cre-Off」系統。在這種設計中,目標基因最初以正確的順序(5'->3')存在,因此在沒有 Cre 的情況下可以表達。它同樣被兩對不同類型的 loxP 位點(例如 loxP 和 lox2272)側翼。
在 Cre 存在時:
當細胞中存在 Cre 重組酶時,Cre 會識別其中一對 loxP 位點,並介導其間 DNA 片段的反轉。這會導致目標基因從正向變為反向。一旦基因被反轉,它就無法被正確轉錄,從而停止表達。與 DIO 類似,第一次反轉後,第二對 loxP 位點也會被切除,確保基因一旦被「關閉」,就無法恢復表達。因此,DO 向量在 Cre 酶存在時會抑制基因表達,實現了「Cre-Off」功能。
在 Cre 不存在時:
在沒有 Cre 重組酶的情況下,DO 向量中的目標基因保持其原始的正向排列。因此,基因會持續被轉錄和翻譯,正常表達其功能。這使得 DO 向量適用於需要在特定細胞類型或發育階段特異性抑制基因表達的研究。
以下表格總結了 DIO 和 DO 向量在 Cre 存在與否時的基因表達結果:
| 向量類型 | 基因初始方向 | Cre 存在時的結果 | Cre 不存在時的結果 | 功能 |
|---|---|---|---|---|
| DIO (Double-floxed Inverted Orientation) | 反向 (3'->5') | 基因反轉為正向,表達開啟 | 基因保持反向,表達關閉 | Cre-On(開啟基因表達) |
| DO (Double-floxed Orientation) | 正向 (5'->3') | 基因反轉為反向,表達關閉 | 基因保持正向,表達開啟 | Cre-Off(關閉基因表達) |
Cre-lox 系統的影響力與挑戰
Cre-lox 重組系統極大地推動了生物醫學研究的進展,尤其是在生成條件性基因敲除或過表達小鼠模型方面。然而,該系統也存在一些挑戰和限制:
- Cre 酶的毒性: 有研究表明,Cre 重組酶在某些細胞中可能引起毒性反應,導致細胞增殖受損甚至死亡,這與其 DNA 鏈切割活性有關。
- 「隱藏」loxP 位點: Cre 酶偶爾會在基因組中天然存在的、與 loxP 序列相似的「隱藏」位點處發生非特異性重組,導致脫靶效應。
- 重組效率不完全: 在某些情況下,Cre 介導的重組可能不是 100% 完全的,特別是當存在兩個拷貝的 floxed 序列時,這可能導致嵌合組織的形成。
- 啟動子特異性: 雖然可利用細胞特異性啟動子來驅動 Cre 表達,但啟動子本身的特異性可能不夠完美,或者受染色體整合位點效應的影響。
儘管存在這些挑戰,科學家們仍在不斷優化 Cre-lox 系統。例如,開發了誘導型 Cre(如他莫昔芬響應的 CreERT)來實現時間上的精確控制,以及結合其他重組酶系統(如 FLP-FRT)來創造更複雜的重組事件,或合成替代的 loxP 位點來指定不同的重組模式。這些進展使得 Cre-lox 系統仍然是基因操作領域中不可或缺的工具。
Cre-lox 系統應用前景評估
為了更直觀地評估 Cre-lox 系統在不同應用領域的表現和潛力,我們將其關鍵特性在雷達圖中呈現。這些特性代表了該系統在基因工程和生物學研究中的多個維度。
雷達圖清晰地展示了 Cre-lox 系統在不同應用中的優勢和潛在的限制。整體而言,它在「精確性」、「靈活性」、「應用廣度」和「時空控制」方面表現出色,尤其在神經科學領域具有極大的影響力。然而,「複雜度」和「脫靶風險」是需要持續關注和優化的方面。Brainbow 技術在「複雜度」和「時空控制」上得分較高,反映了其在細胞標記多樣性方面的卓越能力;而 DIO/DO 開關則在「精確性」和「低脫靶風險」上表現優異,這得益於其明確的基因開關特性。這些特點共同構成了 Cre-lox 系統在現代生物學研究中的強大基礎。
常見問題 (FAQ)
結論
Cre-lox 重組系統無疑是分子生物學和基因工程領域的一項里程碑式創新。從最初在 P1 噬菌體中的發現,到如今廣泛應用於精確控制基因表達和進行細胞追蹤,其影響深遠。Brainbow 系列技術為神經科學提供了前所未有的細胞可視化能力,使科學家能夠解剖複雜的神經迴路;而 DIO 和 DO 向量則為基因功能的條件性研究提供了強大的「開關」機制。儘管存在 Cre 毒性、脫靶重組和重組效率等挑戰,科學家們仍在不斷地優化和擴展其應用。隨著基因編輯技術的不斷發展,Cre-lox 系統將繼續作為一個靈活且不可或缺的工具,推動我們對生命基本過程的理解,並為疾病的治療提供新的策略。
推薦閱讀
- Cre-Lox 系統在基因治療中的應用前景如何?
- Brainbow 技術如何幫助我們理解大腦連結組(Connectome)?
- 比較 Cre-Lox 與 CRISPR-Cas9 基因編輯技術的優劣?
- DIO 和 DO 向量在體內基因表達調控中的實際案例有哪些?
參考文獻
Last updated May 22, 2025