
Desvelando el Mundo de Staphylococcus: Un Informe Microbiológico Detallado
Una inmersión profunda en las características, patogenia y relevancia clínica de este género bacteriano, basada en fuentes expertas.
El género Staphylococcus agrupa a bacterias con una notable importancia tanto en la microbiología comensal como en la patología infecciosa humana y animal. Este informe sintetiza el conocimiento actual sobre estas bacterias, recurriendo a información de textos de referencia como "Koneman's Color Atlas and Textbook of Diagnostic Microbiology" (7ª edición) y "Medical Microbiology" de Patrick R. Murray (8ª edición), así como a recursos de bibliotecas microbiológicas especializadas.
Aspectos Clave de Staphylococcus
- Morfología Distintiva: Los estafilococos son cocos Gram positivos que característicamente se agrupan en forma de racimos de uvas, visibles bajo el microscopio.
- Patógeno Versátil: Staphylococcus aureus es la especie más virulenta y conocida, capaz de causar un amplio espectro de infecciones, desde cutáneas leves hasta sistémicas graves.
- Desafío de Resistencia: La emergencia y diseminación de cepas resistentes a los antibióticos, especialmente S. aureus resistente a la meticilina (SARM o MRSA), representa un problema de salud pública global.
Características Generales del Género Staphylococcus
Los estafilococos son bacterias fascinantes con una serie de características que definen su biología y su interacción con los hospedadores.
Morfología y Estructura Celular
Microscópicamente, los estafilococos son células esféricas (cocos) con un diámetro que oscila entre 0.8 y 1.5 micrómetros. Suelen observarse agrupados irregularmente, formando estructuras que recuerdan a racimos de uvas, aunque también pueden presentarse en parejas o cadenas cortas. Son bacterias Gram positivas, lo que significa que retienen el colorante cristal violeta en la tinción de Gram debido a su gruesa pared de peptidoglicano. Algunas cepas pueden poseer una cápsula externa mucoide, que contribuye a su virulencia al dificultar la fagocitosis. La pared celular también contiene ácidos teicoicos y lipoteicoicos, importantes para la adherencia y la inducción de la respuesta inflamatoria.
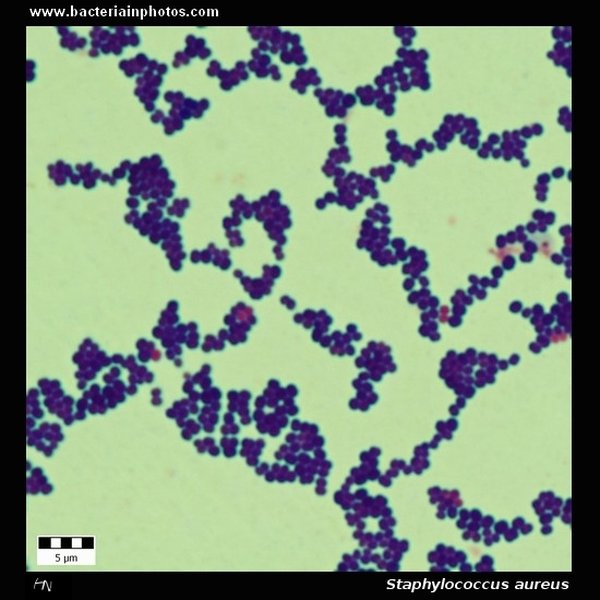
Staphylococcus aureus: tinción de Gram mostrando cocos Gram positivos agrupados en racimos.
Metabolismo y Condiciones de Crecimiento
Los estafilococos son anaerobios facultativos, lo que les confiere la versatilidad de crecer tanto en presencia como en ausencia de oxígeno. Son catalasa positivos, una característica bioquímica clave que los diferencia del género Streptococcus (catalasa negativos). Además, son oxidasa negativos. Crecen con facilidad en la mayoría de los medios de cultivo bacteriológicos estándar, como el agar sangre, donde algunas especies, notablemente S. aureus, pueden producir hemólisis. Una característica distintiva es su capacidad para crecer en medios con altas concentraciones de sal (hasta 6.5-15% de NaCl), como el agar sal manitol, que es selectivo y diferencial para S. aureus. Pueden desarrollarse en un amplio rango de pH y temperaturas, aunque su óptimo suele estar entre 30-37°C. Su contenido de G+C en el ADN varía entre 30-40 mol%.
Especies de Importancia Clínica
Dentro del género Staphylococcus, que incluye más de 40 especies, algunas destacan por su impacto en la salud humana.
Staphylococcus aureus
Es la especie más patógena y estudiada. Se caracteriza por ser coagulasa positiva (una enzima que convierte el fibrinógeno en fibrina, formando un coágulo), fermentar el manitol (visible en agar sal manitol con un viraje de color del indicador) y, frecuentemente, producir una pigmentación dorada en sus colonias (de ahí su nombre "aureus", que significa dorado en latín). S. aureus es responsable de una vasta gama de infecciones, desde afecciones cutáneas como forúnculos, impétigo y celulitis, hasta enfermedades invasivas graves como neumonía, endocarditis, osteomielitis, meningitis y sepsis. También puede causar síndromes mediados por toxinas, como el síndrome de la piel escaldada estafilocócica (SSSS), el síndrome de shock tóxico (TSS) y la intoxicación alimentaria.

Colonias de Staphylococcus aureus en agar tripticasa soja.
Estafilococos Coagulasa-Negativos (ECN o CoNS)
Este grupo heterogéneo incluye especies que son comensales habituales de la piel y mucosas. Aunque generalmente menos virulentos que S. aureus, pueden causar infecciones oportunistas, especialmente en pacientes inmunocomprometidos o aquellos con dispositivos médicos implantados (catéteres, prótesis articulares o valvulares). Las especies más relevantes incluyen:
- Staphylococcus epidermidis: Es el ECN aislado con más frecuencia en infecciones asociadas a dispositivos médicos, debido a su capacidad para formar biopelículas sobre superficies inertes.
- Staphylococcus saprophyticus: Es una causa común de infecciones del tracto urinario (ITU) en mujeres jóvenes sexualmente activas. Se distingue de otros ECN por su resistencia a la novobiocina.
- Staphylococcus haemolyticus: Conocido por su notable resistencia a múltiples antibióticos.
- Staphylococcus lugdunensis: Aunque es coagulasa negativo, puede causar infecciones agresivas similares a las de S. aureus, como endocarditis. Puede expresar un factor de "clumping" similar a la coagulasa ligada.
- Staphylococcus hominis: Es el tercer organismo más común recuperable de la sangre de pacientes inmunocomprometidos.
Diagnóstico Microbiológico
La identificación precisa de las especies de Staphylococcus y la determinación de su perfil de susceptibilidad a los antibióticos son cruciales para el manejo clínico.
Examen Microscópico y Cultivo
La tinción de Gram de muestras clínicas puede revelar la presencia de cocos Gram positivos agrupados en racimos. El cultivo se realiza en medios nutritivos como agar sangre, donde S. aureus típicamente produce colonias redondas, lisas, convexas, de color blanco a amarillo dorado, y a menudo con una zona de beta-hemólisis. Los ECN suelen producir colonias blancas no hemolíticas. El agar sal manitol es un medio selectivo y diferencial: la alta concentración de sal inhibe a la mayoría de las bacterias, excepto a los estafilococos; S. aureus fermenta el manitol, acidificando el medio y haciendo virar el indicador rojo fenol a amarillo.

S. aureus en agar sal manitol, mostrando la fermentación del manitol (colonias amarillas y viraje del medio).
Pruebas Bioquímicas Clave
- Prueba de la catalasa: Todos los estafilococos son catalasa positivos (descomponen el peróxido de hidrógeno en agua y oxígeno, produciendo burbujas). Esta prueba los diferencia de los estreptococos y enterococos (catalasa negativos).
- Prueba de la coagulasa: Es la prueba fundamental para diferenciar S. aureus (coagulasa positivo) de los ECN. Puede realizarse en tubo (detecta coagulasa libre) o en portaobjetos (detecta coagulasa ligada o "clumping factor").
- Sensibilidad a la novobiocina: Útil para identificar S. saprophyticus (resistente) entre los ECN (generalmente sensibles), especialmente en urocultivos.
Métodos Moleculares y Otros
Las técnicas moleculares, como la Reacción en Cadena de la Polimerasa (PCR), se utilizan cada vez más para la detección rápida de S. aureus y genes específicos de virulencia o resistencia, como el gen mecA, que codifica la resistencia a la meticilina (en SARM). La espectrometría de masas MALDI-TOF se ha convertido en una herramienta estándar en muchos laboratorios para la identificación rápida y precisa de especies bacterianas, incluyendo estafilococos.
Comparativa de Especies Relevantes de Staphylococcus
La siguiente tabla resume algunas características distintivas de las especies de Staphylococcus más comunes en la clínica, ayudando a comprender sus diferencias y similitudes en el diagnóstico y la patogenia.
| Característica | Staphylococcus aureus | Staphylococcus epidermidis | Staphylococcus saprophyticus |
|---|---|---|---|
| Coagulasa | Positivo | Negativo | Negativo |
| Fermentación de Manitol | Positivo | Negativo (generalmente) | Variable (a menudo negativo o débil) |
| Hemólisis en Agar Sangre | Beta (generalmente) | Gamma (no hemolítico) | Gamma (no hemolítico) |
| Pigmento | Dorado (variable) | Blanco | Blanco/Amarillo pálido |
| Sensibilidad a Novobiocina | Sensible | Sensible | Resistente |
| Infecciones Comunes | Piel y tejidos blandos, neumonía, sepsis, endocarditis, osteomielitis, intoxicación alimentaria, TSS | Infecciones asociadas a dispositivos (catéteres, prótesis), bacteriemia en inmunocomprometidos | Infecciones del tracto urinario (especialmente en mujeres jóvenes) |
| Formación de Biopelícula | Sí | Fuerte capacidad | Sí (menos prominente que S. epidermidis) |
Patogenia y Factores de Virulencia
La capacidad de los estafilococos, especialmente S. aureus, para causar enfermedad se debe a un arsenal de factores de virulencia.
Componentes Estructurales
- Cápsula: Presente en algunas cepas, interfiere con la fagocitosis.
- Pared celular (Peptidoglicano y Ácidos Teicoicos): El peptidoglicano tiene actividad tipo endotoxina e induce la liberación de citoquinas. Los ácidos teicoicos (especialmente el ácido lipoteicoico) median la adherencia a las células del hospedador.
- Proteína A (en S. aureus): Se une a la porción Fc de las inmunoglobulinas IgG, inhibiendo la opsonización y la fagocitosis.
- Proteínas de Adhesión (MSCRAMMs): Moléculas de superficie que reconocen componentes de la matriz celular del hospedador (ej. fibronectina, fibrinógeno, colágeno), facilitando la colonización y la invasión tisular.
Enzimas Extracelulares
- Coagulasa: Convierte fibrinógeno en fibrina, formando un coágulo que puede proteger a la bacteria de las defensas del hospedador.
- Catalasa: Neutraliza el peróxido de hidrógeno, protegiendo a la bacteria del estallido respiratorio de los fagocitos.
- Hialuronidasa: Degrada el ácido hialurónico del tejido conectivo, facilitando la diseminación bacteriana.
- Fibrinolisina (Estafiloquinasa): Disuelve los coágulos de fibrina, permitiendo la propagación.
- Lipasas: Hidrolizan lípidos, permitiendo la supervivencia en áreas sebáceas de la piel y la invasión de tejidos.
- Nucleasas: Degradan el ADN y ARN, lo que podría ayudar a evadir las trampas extracelulares de neutrófilos (NETs).
Toxinas
- Citotoxinas (Hemolisinas alfa, beta, gamma, delta y Leucocidina de Panton-Valentine - PVL): Dañan las membranas celulares de diversos tipos de células, incluyendo eritrocitos, leucocitos y plaquetas. La PVL está asociada con infecciones cutáneas graves y neumonía necrosante.
- Toxinas Exfoliativas (ETA, ETB): Causan el síndrome de la piel escaldada estafilocócica (SSSS) al romper los puentes intercelulares (desmogleína-1) en la epidermis.
- Enterotoxinas (A-E, G-X): Son superantígenos termoestables responsables de la intoxicación alimentaria estafilocócica (vómitos y diarrea).
- Toxina del Síndrome de Shock Tóxico (TSST-1): Es un superantígeno que causa una activación masiva de linfocitos T, llevando a una liberación exagerada de citoquinas y al desarrollo del síndrome de shock tóxico.
Formación de Biopelículas
Muchas especies de Staphylococcus, en particular S. epidermidis y S. aureus, son capaces de formar biopelículas. Estas son comunidades bacterianas embebidas en una matriz autoproducida de exopolisacáridos, proteínas y ADN extracelular, que se adhieren a superficies bióticas (tejidos) o abióticas (dispositivos médicos). Las bacterias dentro de las biopelículas son más resistentes a los antibióticos y a las defensas del hospedador, lo que las hace difíciles de erradicar y contribuye a la cronicidad de las infecciones.
Visualización Comparativa de Factores Clave en Staphylococcus
El siguiente gráfico de radar ofrece una representación visual comparativa de la expresión relativa de ciertos factores importantes (patogenicidad, potencial de resistencia, formación de biopelícula y producción de toxinas) entre Staphylococcus aureus, Staphylococcus epidermidis y Staphylococcus saprophyticus. Esta es una evaluación cualitativa basada en el conocimiento general de estas especies, donde una puntuación más alta indica una mayor prominencia del factor.
Este gráfico ilustra cómo S. aureus generalmente presenta una mayor patogenicidad y producción de toxinas, mientras que S. epidermidis destaca por su capacidad de formar biopelículas. S. saprophyticus, aunque menos virulento en general, tiene una notable capacidad de adherencia en el tracto urinario.
Resistencia a los Antibióticos
La resistencia a los antibióticos en Staphylococcus es un problema creciente y de gran preocupación.
Resistencia a la Penicilina
Poco después de la introducción de la penicilina, la mayoría de las cepas de S. aureus desarrollaron resistencia mediante la producción de la enzima β-lactamasa, que hidroliza el anillo β-lactámico de la penicilina, inactivándola.
Staphylococcus aureus Resistente a la Meticilina (SARM o MRSA)
La meticilina (y otras penicilinas resistentes a la β-lactamasa como la oxacilina y la cloxacilina) se desarrollaron para tratar estas infecciones. Sin embargo, pronto emergieron cepas de SARM. La resistencia a la meticilina se debe a la adquisición del gen mecA (o más raramente mecC), que codifica una proteína de unión a la penicilina alterada, PBP2a (o PBP2c). PBP2a tiene baja afinidad por los antibióticos β-lactámicos, permitiendo la síntesis de la pared celular incluso en presencia de estos fármacos. El gen mecA se encuentra en un elemento genético móvil llamado casete cromosómico estafilocócico mec (SCCmec). El SARM es resistente a todos los antibióticos β-lactámicos, incluyendo cefalosporinas y carbapenems (con algunas excepciones de cefalosporinas de nueva generación activas contra SARM). Las infecciones por SARM son un desafío terapéutico importante, tanto en hospitales (SARM-AH) como en la comunidad (SARM-AC).
Otras Resistencias
Los estafilococos también pueden desarrollar resistencia a otros antimicrobianos, como macrólidos, lincosamidas, aminoglucósidos, tetraciclinas y fluoroquinolonas. La vancomicina ha sido el tratamiento de elección para infecciones graves por SARM, pero han surgido cepas con sensibilidad reducida (VISA - S. aureus con sensibilidad intermedia a vancomicina) e incluso resistencia (VRSA - S. aureus resistente a vancomicina), aunque estas últimas son raras. La aparición de VRSA es particularmente alarmante, ya que limita drásticamente las opciones terapéuticas.
Mapa Conceptual de Staphylococcus
Para una visión general de los aspectos clave del género Staphylococcus, el siguiente mapa mental resume sus características, especies importantes, mecanismos de patogenia, tipos de infecciones, diagnóstico y la problemática de la resistencia antibiótica.
Este diagrama ayuda a conectar los diferentes conceptos relacionados con Staphylococcus, desde sus propiedades básicas hasta su impacto clínico.
Reservorio y Transmisión
Los estafilococos son comensales comunes de la piel y las mucosas (especialmente las fosas nasales anteriores) de humanos y animales de sangre caliente. Aproximadamente el 20-30% de la población sana es portadora persistente de S. aureus en las fosas nasales, mientras que otros son portadores intermitentes o no portadores. También pueden encontrarse en el ambiente, alimentos y agua contaminada. La transmisión ocurre principalmente por contacto directo con personas colonizadas o infectadas, o a través de fómites (objetos contaminados). Las manos son un vehículo importante de transmisión. Las autoinfecciones también son comunes, donde la propia flora del individuo causa una infección, a menudo tras una ruptura de la barrera cutánea o mucosa (heridas, cirugías, uso de dispositivos médicos).
Video Explicativo sobre Staphylococci
Para complementar la información textual, el siguiente video de Lecturio ofrece una visión general sobre la microbiología de los estafilococos, abordando su estructura, virulencia, patogenia y epidemiología de las enfermedades asociadas. Este recurso visual puede ayudar a consolidar la comprensión de los conceptos clave discutidos en este informe.
El video profundiza en cómo estos microorganismos interactúan con el huésped y los mecanismos que utilizan para causar enfermedades, lo cual es fundamental para entender la relevancia clínica de Staphylococcus.
Preguntas Frecuentes (FAQ)
Consultas Recomendadas para Profundizar
- ¿Cuáles son los mecanismos moleculares detallados de la formación de biopelículas en Staphylococcus epidermidis?
- Explorar las diferencias epidemiológicas y de virulencia entre SARM adquirido en la comunidad (SARM-AC) y SARM adquirido en el hospital (SARM-AH).
- Investigar las estrategias terapéuticas más recientes y en desarrollo para combatir las infecciones por Staphylococcus resistentes a múltiples fármacos.
- ¿Cómo funcionan las toxinas superantigénicas de Staphylococcus aureus como TSST-1 a nivel inmunológico?
Referencias
Last updated May 14, 2025