
Enterococos: Un Análisis Profundo de su Resistencia Antimicrobiana y Relevancia Clínica
Desentrañando los secretos de uno de los patógenos nosocomiales más desafiantes
Los enterococos, bacterias grampositivas que habitan comúnmente en el tracto gastrointestinal humano y animal, representan un desafío creciente en la medicina moderna debido a su notable capacidad de desarrollar y adquirir resistencia a múltiples antibióticos. Originalmente clasificados dentro del género Streptococcus, estos microorganismos han evolucionado hasta convertirse en patógenos nosocomiales prominentes, responsables de una amplia gama de infecciones que incluyen infecciones del tracto urinario (ITU), endocarditis y sepsis. Su comprensión es crucial para el diagnóstico y tratamiento efectivos en el ámbito clínico.
Puntos Clave sobre los Enterococos y su Resistencia
- Clasificación Serológica Fundamental: La clasificación de Lancefield, aunque históricamente agrupara a los enterococos dentro del grupo D de Streptococcus, sigue siendo un pilar para entender sus características antigénicas, incluso después de su reclasificación como un género separado.
- Resistencia Intrínseca y Adquirida: Los enterococos poseen una resistencia natural significativa a varias clases de antibióticos, como las cefalosporinas y los aminoglucósidos, y han desarrollado la capacidad de adquirir nuevas resistencias a fármacos de última línea como la vancomicina, lo que los convierte en patógenos de difícil manejo.
- Factores de Virulencia Multifacéticos: Aunque considerados de baja virulencia intrínseca, los enterococos emplean una variedad de factores como la proteína de superficie extracelular (Esp) y la citolisina para adherirse, colonizar tejidos y evadir la respuesta inmune del huésped, contribuyendo a la patogénesis de las infecciones.
Introducción a los Enterococos: Generalidades y Comportamiento
Los enterococos son cocos grampositivos, anaerobios facultativos, que se presentan típicamente en parejas o cadenas cortas, aunque ocasionalmente pueden formar cadenas largas. Son notablemente resilientes, capaces de crecer en una amplia gama de temperaturas (10-45 °C), en medios salinos o con pH alcalino, y en presencia de bilis. Estas características les permiten sobrevivir en diversos entornos, incluidos los hospitalarios, lo que contribuye a su papel como patógenos nosocomiales. Las especies más relevantes clínicamente son Enterococcus faecalis y Enterococcus faecium, siendo E. faecalis la más frecuente en infecciones humanas, aunque E. faecium es a menudo la especie más resistente.
La Clasificación de Rebecca Lancefield: Un Hito en Microbiología
La Dra. Rebecca Craighill Lancefield revolucionó la microbiología con su sistema de clasificación serológica de los estreptococos β-hemolíticos, basado en la naturaleza antigénica de los carbohidratos de su pared celular. Aunque los enterococos (originalmente Streptococcus del grupo D) se clasifican ahora como un género distinto (Enterococcus), conservan la expresión del antígeno del grupo D de Lancefield. Esta clasificación fue crucial para diferenciar y estudiar las diversas especies de estreptococos, lo que permitió una mejor comprensión de su patogenicidad y epidemiología.

Microscopía de Enterococcus faecalis, mostrando su morfología cocoide.
Morfología y Microscopía de los Enterococos
Al observar los enterococos bajo el microscopio, se aprecian como cocos grampositivos, lo que significa que retienen la tinción de Gram, apareciendo de color violeta o azul. Su disposición característica en pares o cadenas cortas es un rasgo distintivo que ayuda a su identificación inicial. En el laboratorio clínico, la tinción de Gram es el primer paso en la identificación microscópica de estas bacterias.
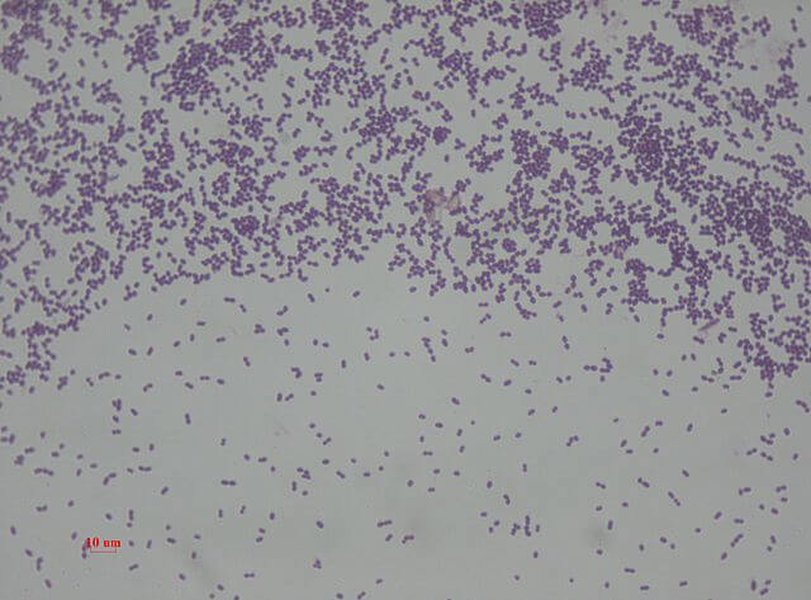
Tinción de Gram de Enterococcus faecalis, revelando su naturaleza grampositiva.
Hábitat y Estructura Antigénica
El hábitat principal de los enterococos es el tracto gastrointestinal de humanos y animales, donde forman parte de la microbiota normal. También pueden encontrarse en productos lácteos y otros alimentos. Su estructura antigénica se define principalmente por el polisacárido de la pared celular que comparte características con el antígeno del grupo D de Lancefield. Esta característica es clave para su identificación serológica, aunque ahora se consideren un género aparte de Streptococcus.
Factores de Virulencia y Mecanismos de Patogenicidad
Aunque no se consideran altamente virulentos en comparación con otros patógenos, los enterococos poseen varios factores que contribuyen a su capacidad para causar infecciones, especialmente en individuos inmunocomprometidos o con condiciones subyacentes.
Factores de Virulencia Clave
- Proteína de Superficie Extracelular (Esp): Promueve la adhesión a las células del huésped y la formación de biopelículas, lo que facilita la colonización y la evasión del sistema inmune. Se ha asociado también con la resistencia antimicrobiana.
- Citolisina (Cyl) o Hemolisina: Esta toxina posee propiedades beta-hemolíticas en humanos y es bactericida contra otras bacterias grampositivas, contribuyendo al daño tisular y a la competencia en el microambiente.
- Gelatinasa (GelE): Una proteasa extracelular que hidroliza proteínas como la gelatina, la caseína y el colágeno, facilitando la invasión y el daño tisular.
- Agregación de Sustancias (AS): Factor que promueve la adhesión entre las bacterias y a las células del huésped, además de estar implicado en la formación de biopelículas.
- Antígeno Específico de Endocarditis A (EfaA): Un factor de adhesión asociado con la capacidad de E. faecalis de causar endocarditis.
Mecanismos de Patogenicidad
Los enterococos causan infecciones aprovechando su capacidad para colonizar y persistir en diversos nichos anatómicos, especialmente en pacientes con hospitalización prolongada, uso de dispositivos invasivos o terapia antibiótica previa. Sus factores de virulencia les permiten adherirse a superficies bióticas y abióticas, formar biopelículas que los protegen de los antibióticos y de la respuesta inmune, y secretar enzimas y toxinas que contribuyen al daño tisular y la diseminación. Las infecciones comunes incluyen ITU, bacteriemias, endocarditis, infecciones de heridas y abscesos profundos.
La Batalla contra la Resistencia Antimicrobiana
La resistencia antimicrobiana en enterococos es una preocupación global. Poseen una resistencia intrínseca a varias clases de antibióticos y una notable capacidad para adquirir nuevos genes de resistencia a través de plásmidos y transposones, lo que dificulta significativamente el tratamiento.
Tipos de Resistencia en Enterococos
Resistencia Intrínseca
- Beta-lactámicos: Los enterococos son intrínsecamente resistentes a muchas cefalosporinas, aztreonam y penicilinas antiestafilocócicas (como la nafcilina y la oxacilina) debido a la baja afinidad de sus proteínas de unión a penicilinas (PBP), como la PBP-4.
- Aminoglucósidos: Presentan resistencia de bajo nivel a los aminoglucósidos, lo que los hace ineficaces como monoterapia. Para lograr un efecto bactericida, se requiere la combinación con un antibiótico que actúe sobre la pared celular.
- Lincosamidas: Resistencia intrínseca a lincomicina y clindamicina.
Resistencia Adquirida
- Resistencia de Alto Nivel a Aminoglucósidos (HLAR): Se debe a la producción de enzimas inactivantes de antibióticos, anulando el efecto sinérgico con beta-lactámicos o glucopéptidos.
- Resistencia a Vancomicina (ERV): La resistencia a la vancomicina es uno de los problemas más apremiantes. Cepas de ERV son difíciles de tratar debido a la limitación de opciones antibióticas. Esta resistencia se media principalmente por el operón van, que altera el blanco del antibiótico en la pared celular. E. faecium es particularmente propenso a desarrollar resistencia a vancomicina y ampicilina.
- Resistencia a Ampicilina: Especialmente común en E. faecium, limitando las opciones de tratamiento para esta especie.
El siguiente gráfico de radar ilustra la complejidad de la resistencia a los antibióticos en las dos especies de Enterococcus más relevantes clínicamente, destacando las diferencias en su perfil de susceptibilidad.
Como se puede observar en el gráfico, Enterococcus faecium tiende a mostrar patrones de resistencia significativamente más altos a antibióticos clave como la ampicilina, la vancomicina y la teicoplanina, en comparación con Enterococcus faecalis. Esto subraya por qué E. faecium es un patógeno de mayor preocupación en el contexto de la resistencia antimicrobiana y un desafío terapéutico más grande.
Algoritmo de Trabajo en el Laboratorio Clínico y Antibiograma
El diagnóstico preciso y la determinación de la susceptibilidad antimicrobiana son fundamentales para guiar el tratamiento de las infecciones por enterococos.
Diagnóstico en el Laboratorio
El algoritmo de trabajo en el laboratorio clínico para la identificación de enterococos generalmente sigue estos pasos:
- Recolección de Muestras: Dependiendo del sitio de la infección (orina, sangre, heridas, etc.).
- Tinción de Gram: Observación de cocos grampositivos en parejas o cadenas cortas.
- Cultivo: Siembra en medios de cultivo apropiados. Los enterococos crecen bien en agar sangre y pueden tolerar medios con bilis-esculina, donde hidrolizan la esculina, produciendo un ennegrecimiento del medio.
- Pruebas Bioquímicas:
- Catalasa: Negativa (para diferenciarlos de estafilococos).
- Crecimiento en NaCl 6.5%: Positivo (diferenciándolos de muchos estreptococos).
- Hidrólisis de Esculina en Bilis: Positivo.
- PYR (Pirrolidonil arilamidasa): Positivo (prueba rápida para identificación presuntiva de Enterococcus y Streptococcus pyogenes).
- Identificación a Nivel de Especie: Se realizan pruebas bioquímicas adicionales o métodos moleculares (como PCR o espectrometría de masas MALDI-TOF) para diferenciar entre E. faecalis, E. faecium y otras especies menos comunes.
Antibiograma: Determinación de la Susceptibilidad Antimicrobiana
El antibiograma es esencial para seleccionar el tratamiento adecuado, dada la complejidad de la resistencia de los enterococos. Se utilizan métodos estandarizados como la difusión en disco (Kirby-Bauer) o la microdilución en caldo para determinar la concentración mínima inhibitoria (CMI) de diversos antibióticos.

Un antibiograma, mostrando los halos de inhibición alrededor de los discos de antibióticos.
Se evalúa la susceptibilidad a antibióticos clave como:
- Beta-lactámicos: Ampicilina, penicilina G (especialmente para E. faecalis).
- Glucopéptidos: Vancomicina, teicoplanina (vigilando la aparición de ERV).
- Aminoglucósidos: Gentamicina y estreptomicina (para evaluar la resistencia de alto nivel y la necesidad de terapia combinada).
- Otros: Linezolid, daptomicina, tigeciclina (opciones para cepas multirresistentes, especialmente ERV), nitrofurantoína (para ITU no complicadas).
La interpretación de los resultados del antibiograma es crítica, ya que los enterococos pueden ser tolerantes o mostrar sinergia con combinaciones de antibióticos.
A continuación, se presenta una tabla que resume los patrones de resistencia y opciones de tratamiento para las principales especies de enterococos:
| Especie de Enterococo | Resistencia Intrínseca Común | Resistencia Adquirida Preocupante | Opciones Terapéuticas Clave (Si es Sensible) | Opciones Terapéuticas para Cepas Resistentes |
|---|---|---|---|---|
| Enterococcus faecalis | Cefalosporinas, Aztreonam, Penicilinas antiestafilocócicas, Resistencia de bajo nivel a aminoglucósidos | HLAR, Resistencia a vancomicina (menos frecuente que en E. faecium) | Ampicilina o Penicilina G (con o sin aminoglucósido para infecciones graves), Vancomicina, Nitrofurantoína (ITU) | Linezolid, Daptomicina, Tigeciclina |
| Enterococcus faecium | Resistencia inherente a ampicilina, Cefalosporinas, Aztreonam, Penicilinas antiestafilocócicas, Resistencia de bajo nivel a aminoglucósidos | HLAR, Resistencia a vancomicina (ERV, muy frecuente), Resistencia a quinolonas | Vancomicina (si es sensible), Linezolid, Daptomicina, Tigeciclina, Quinupristina/Dalfopristina (solo para algunas cepas de E. faecium) | Linezolid, Daptomicina, Tigeciclina (tratamiento de ERV es un reto) |
Es importante destacar que el tratamiento de las infecciones por enterococos resistentes, especialmente los ERV, es un desafío significativo, y se requiere una vigilancia continua de los patrones de resistencia para optimizar las estrategias terapéuticas.
Video sobre Mecanismos y Bases Genéticas de la Resistencia al Uso de Antimicrobianos. Este video proporciona una excelente visión general de cómo las bacterias desarrollan resistencia, un factor crítico en el manejo de infecciones por enterococos.
Preguntas Frecuentes (FAQ)
Conclusión
Los enterococos son patógenos bacterianos versátiles y adaptables que plantean un desafío significativo en la práctica clínica debido a su resistencia intrínseca y adquirida a múltiples antibióticos. Su comprensión, desde la clasificación histórica de Lancefield hasta los complejos mecanismos de virulencia y resistencia, es esencial para el diagnóstico y el tratamiento efectivos. La vigilancia continua de los patrones de resistencia y el desarrollo de nuevas estrategias terapéuticas son imperativos para combatir la creciente amenaza de estas bacterias multirresistentes.
Preguntas Relacionadas para Profundizar
- ¿Cuáles son los mecanismos moleculares de resistencia a vancomicina en Enterococcus?
- ¿Cómo impactan las biopelículas de Enterococcus en las infecciones crónicas?
- ¿Qué nuevas estrategias terapéuticas existen para Enterococcus multirresistentes?
- ¿Cuál es la epidemiología de Enterococcus resistentes a antibióticos en el ámbito hospitalario?